目录氯化铝的性质和用途 氢氧化铝性状 氢氧化铝的熔点是多少 氢氧化铝有较强的什么性质 铝物理性质

氢谨物氧化铝是白色胶装物,不溶于水,吸附性祥瞎液强。虽然是两性氢氧化物,但只与强酸强碱反应神消,很难与弱酸弱碱反应。

铝的重要化合物
1、氧化铝(Al2O3)
(1)物理性质:白色固体、熔点高(2054℃)
、不溶于水,不与水化合。常作耐火材料。
刚玉的主要成分是Al2O3
,其中把含少量铬元素的刚玉称为红宝石;含少量的铁和钛元素的刚玉称为蓝宝石。(2)化学性质:①电解熔融的氧化铝制备单质铝但由于氧化铝的熔点很高,故在氧化铝搏碰中添加冰晶石(Na3AlF6)降低其熔点。电解
2Al2O3
=========
2Al
+
3
O2
↑②与酸反应:Al2O3+6HCl=AlCl3+3H2O③世禅与碱反应:Al2O3+2NaOH=2NaAlO2+H2O既能与酸反应又搜银尘能与碱反应生成盐和水的氧化物叫两性氧化物2、氢氧化铝(Al(OH)3)(1)物理性质:氢氧化铝是白色胶状物质,不溶于水,有强的吸附性,可以吸附水中的悬浮物和各种色素。(2)化学性质:①不稳定性:氢氧化铝不稳定,受热易分解。
△
2Al(OH)3
=
Al2O3+2H2O
这是工业上制取纯净氧化铝的方法。
②Al(OH)3+NaOH=
NaAlO2+2H2O③Al(OH)3
+
3HCl=
AlCl3
+
3H2O
Al(OH)3
具有两性的原因:H++AlO2—+H2O
Al(OH)3
Al3+
+
3OH—注意:(1)氢氧化铝作为碱时是三元碱;作为酸时是一元酸(HAlO3)。
(2)氢氧化铝与酸碱反应时,弱酸弱碱是不能把氢氧化铝溶解的。3、明矾:KAl(SO4)2·12H2O复盐的概念:由两种不同的金属离子和一种酸根离子组成的盐叫复盐。
KAl(SO4)2
=K++Al3++2SO42-
Al3++3H2O
======
Al(OH)3
(胶体)
+3H+
△
氢氧化铝性质氢氧化铝(Aluminum hydroxide),化学式Al(OH)3,是铝的氢氧化物。氢氧化铝既能袜亏与酸反应生成盐和水又能与强碱反应生成盐和水,因此也是一种两性氢氧化物。化学式Al(OH)3,是铝的氢氧化物。是一种碱,由于又显一定的酸性,所以又可称之为铝酸(H3AlO3)。但实际与碱反应简高时告咐神生成的是四羟基合铝酸盐([Al(OH)4]-)。因此通常在把它视作一水合偏铝酸(HAlO2·H2O),按用途分为工业级和医药级两种。
氢氧化铝(Aluminium hydroxide),化学式Al(OH)3,是铝的氢氧化物。氢氧化铝既能与酸反应生成盐和水又能与强碱反应生成盐和水,因此也是一种两性氢氧化物。化学式Al(OH)3,是铝的氢氧化物。由于又显一定的酸性,所以又可称之为铝酸(H3AlO3)。但实际与碱反应时生成的是四羟基合铝酸盐([Al(OH)4]-)。因此通常在把它视作一水合偏铝酸携脊(HAlO2·H2O),按用途分为工业级和医药级两种。
物化性质
外观与性状:白色非晶形的粉末
密度:2.40
熔点:300℃
水溶解性:难溶
储存条件:库房通风低温干燥
抗酸作用慢、持久、较强,有收敛作用,有粘膜保护作用,导致便秘,不产生CO2(二氧化碳),无酸反 跳,无碱血症。
氢氧辩腊渗化铝与酸反应:Al(OH)3+3HCl →AlCl3+3H2O
Al(OH)3+3H+ →Al3++3H2O
氢氧化铝与碱反应:Al(OH)3+NaOH → Na[Al(OH)4]
氢氧化铝在碱性环境中异构反应:Al(OH)3→HAlO2+H2O
Al(OH)3+OH-→AlO2-+2H2O
氢氧化铝受热分解:2Al(OH)3==加热==Al2O3+3H2O
氢氧化铝水中两种电离:
1、Al(OH)3⇋Al3++ 3OH-(碱式电离)
2、Al(OH)3+H2O⇋[Al(OH)4]-+H+(酸式电离)
其中的[Al(OH)4]-中学上习惯写成AlO2-,但是实际上这是错误的。
一般所谓的氢氧化铝实际上是指三氧化二铝的水合物。如向铝盐溶液中加入氨水或弱碱而得到的白色胶状沉淀,其含水量不定,组成也不均匀,统称为水合氧化铝。只有在铝酸盐溶液中(含有Al(OH)4-离子)的溶液中通CO2才可得到真正的氢氧化铝。
结晶的氢氧化铝与水合氧化铝不同,难溶于酸,加热到373K也不脱水,在573K加热2h才能转变为偏氢氧化铝(AlO(OH))。
氢氧化铝属两性氢氧化物。由于其存在两种电离形式,既是弱酸,可以有酸式化学式H3AlO3,又是弱碱,可以有碱式化学式Al(OH)3。氢氧化铝具有两性,既能与酸反应又能与碱反应。
氢氧化铝的酸性在于它是路易斯酸可以加合OH-,从而体现碱性
Al(OH)3由于两种电离的存在,可以产生两种盐:铝盐和偏铝酸盐:
⒈铝盐:Al3+AlCl3,KAl(SO4)2·12H2O(明矾)。它们的水溶液因Al3+的水解而显酸性
2.偏铝酸盐,AlO-NaAlO2,KAlO2.它们的水溶液呈碱性:AlO-+ 2H2O → Al(OH)3+ OH-当两类盐混合时,即发生双水解反应,生成 Al(OH)3
Al3++ 3 AlO-+ 6H2O == 4Al(OH)3↓
氢氧化铝主要有325目、800目、1250目、5000目四个规格。白色局租粉末状固体。几乎不溶于水,能凝聚水中的悬浮物,吸附色素。
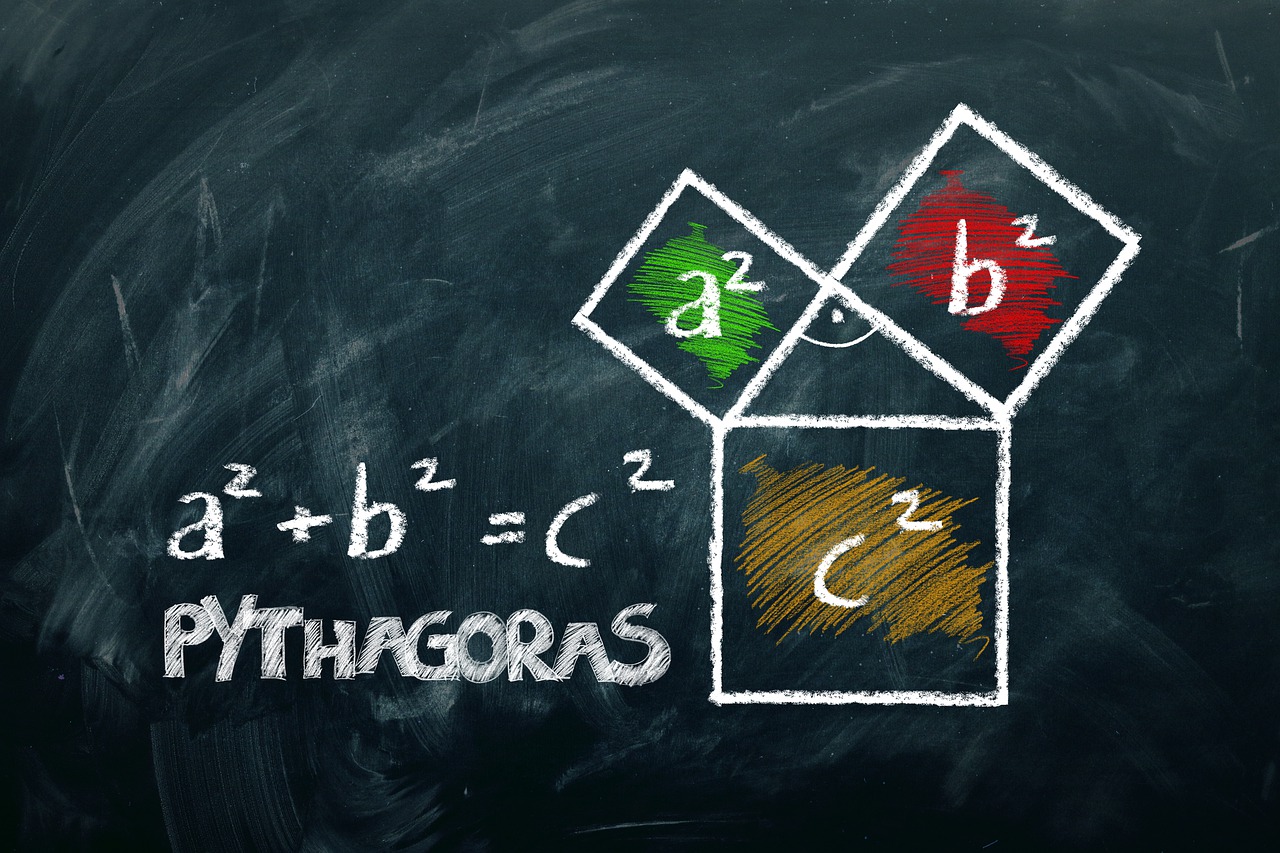
还不备则了解氢氧化铝的小伙伴烂滚指快来瞧瞧吧!,下面由我为你精心准备了“氢氧化铝是沉淀吗?氢氧化铝的物理性质”,持饥配续关注本站将可以持续获取更多的考试资讯!
氢氧化铝是沉淀吗?氢氧化铝的物理性质
氢氧化铝是沉淀 , 氢氧化铝沉淀形态是白色胶状沉淀 。氢氧化铝化学式Al(OH)3,是铝的氢氧化物。氢氧化铝既能与酸反应生成盐和水又能与强碱反应生成盐和水,因此它是一种两性氢氧化物。由于又显一定的酸性,所以又可称之为铝酸(H3AlO3)。但实际与碱反应时生成的是四羟基合铝酸盐([Al(OH)4]-)。
物理性质
一种白色胶状物质,几乎不溶于水。抗酸作用慢、持久、较强,有收敛作用,有粘膜保护作用,导致便秘,不产生CO2(二氧化碳),无酸反跳,无碱血症。
实验室制法
化学方程式:2Al+3H2SO4(稀)=Al2(SO4)3+3H2↑
2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑
Al2(SO4)3+6Na[Al(OH)4]+12H2O=8Al(OH)3↓+3Na2(SO4)或
Al2(SO4)3+6NH3.H2O=2Al(OH)3↓+3(NH4)2SO4
离子方程式:2Al+6H+=2Al3++3H2↑
2Al3++2OH-+6H2O=2[Al(OH)4]-+3H2↑
Al3++3[Al(OH)4]-+6H2O=4Al(OH)3↓
或Al3++3NH3·H2O=Al(OH)3↓+3NH4+
①Al(OH)3是两性氢氧化物,在常温下它既能与强酸,又能与强碱反应:
Al(OH)3+3HCl=AlCl3+3H2O Al(OH)3+3H+=Al3++3H2O
Al(OH)3+NaOH=Na[Al(OH)4]Al(OH)3+OH-=[Al(OH)4]-
②Al(OH)3受热易分解成Al2O3:2Al(OH)3==Al2O3+3H2O(规律:不溶性碱受热均会分解)
③Al(OH)3的制备:
a、可溶性铝盐和氨水反应来制备Al(OH)3
AlCl3+3NH3·H2O=Al(OH)3↓+3NH4Cl
Al2(SO4)3+6NH3·H2O=2 Al(OH)3↓+3(NH4)2SO4(Al3++3NH3·H2O=Al(OH)3↓+3NH4+)
因为强碱(如NaOH)易与Al(OH)3反应,所以实验室不用强碱制备Al(OH)3,而用氨水
b、四羟基合铝酸钠与过量二氧化碳反应
Na[Al(OH)4]+CO2(过)=NaHCO3+Al(OH)3↓
过量的二氧化碳不与氢氧化铝反应,保证[Al(OH)4]-全部生成氢氧化铝